انواع محلول ها از نظر انحلالیت پذیری
محلول ها بر اساس مقدار ماده حل شونده در محلل به سه دسته طبقه بندی میشوند:
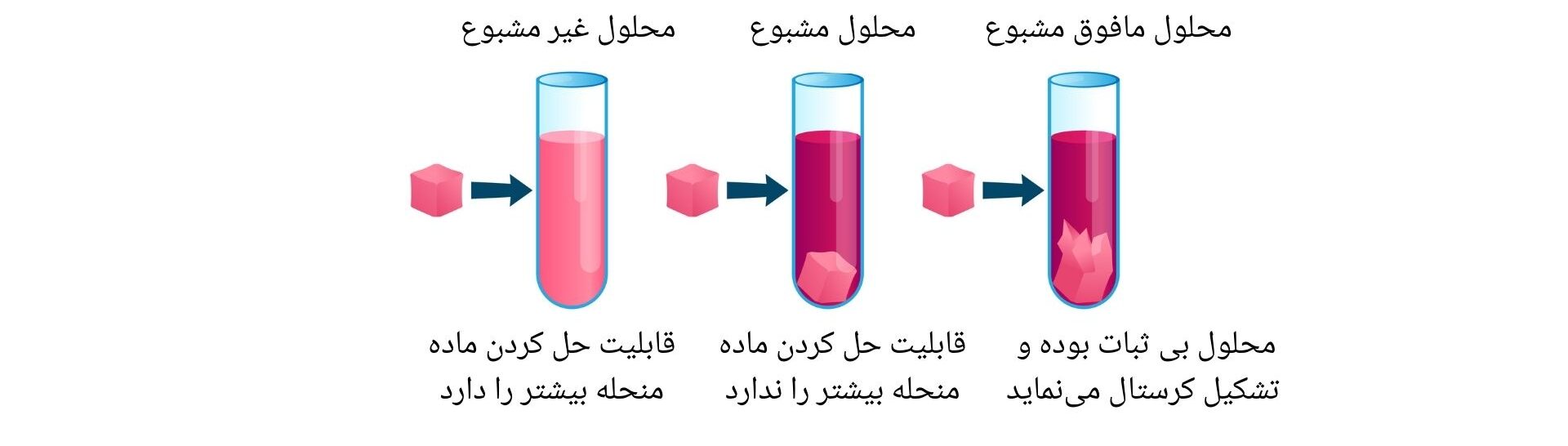
- محلول مشبوع (Saturated Solution): به محلولی گفته میشود که در آن بیشترین حد ممکن ماده حل شونده در ماده حل کننده، در یک درجه حرارت معین حل شده باشد، به گونه ایکه امکان حل شدن بیشتر ماده حل شونده در حلال وجود نداشته باشد. چنین محلول را بنام محلول مشبوع مینامند.
- محلول ما فوق مشبوع (Supersaturated Solution): محلولی مشبوعی که در اثر عوامل خارجی مانند حرارت و فشار مقدار بیشتری از مواد منحله را در خود حل کنند. در این حالت اگر مقدار ماده منحله بیشتر از ظرفیت محلول مشبوع باشد، بخشی از آن رسوب میکند. این نوع محلول را محلول مافوق مشبوع گویند.
- محلول غیر مشبوع (Unsaturated Solution): محلولی است که در آن، حلال توانایی حل کردن مقدار بیشتر از ماده حل شونده را در خود داشته باشند.
تصویر ذیل نشان دهنده محلول های مشبوع، غیرمشبوع و مافوق مشبوع اند.
 همچنان بر اساس اندازه ماده منحله موجود در یک محلول، از اصطلاحات (محلول غلیظ) و (محلول رقیق) استفاده میشود. که این اصطلاحات به توصیف کیفی محلول ها کمک میکنند، اما برای توصیف کمی از روش های محاسباتی دقیق تری استفاده میکنند.
همچنان بر اساس اندازه ماده منحله موجود در یک محلول، از اصطلاحات (محلول غلیظ) و (محلول رقیق) استفاده میشود. که این اصطلاحات به توصیف کیفی محلول ها کمک میکنند، اما برای توصیف کمی از روش های محاسباتی دقیق تری استفاده میکنند.
در این ویدیو در ارتباط با تاثیر حرارت بالای انحلالیت مواد کار شده است.
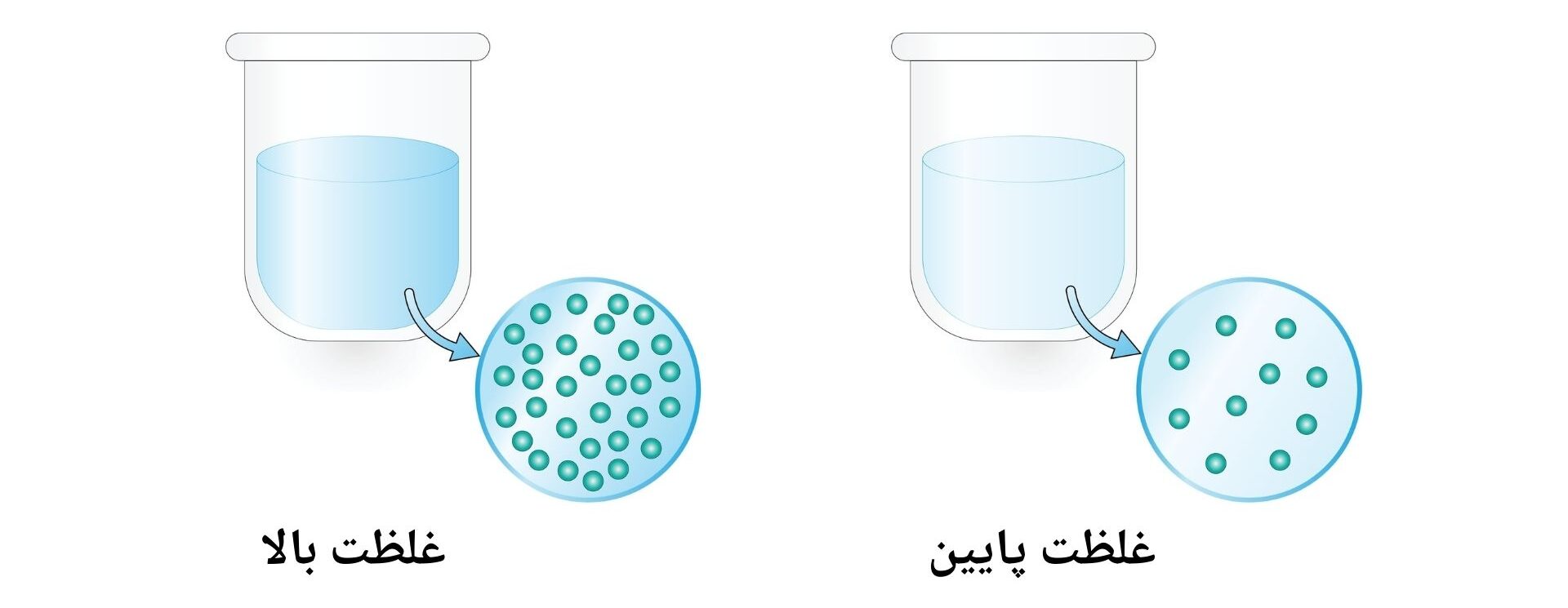
محلول غلیظ: به محلولی گفته می شوند که مقدار زیادی ماده منحله را در مقدار مشخص از محلل، حل شده باشد.
محلول رقیق: به محلولی گفته می شود که از حل ساختن مقدار کمی مانده منحله در یک مقدار مشخص از محلل تشکیل می گردد.
تصاویر ذیل نشان دهنده محلول های رقیق و غلیظ می باشند.
 محلول ها از نگاه کاربرد و ترکیب:
محلول ها از نگاه کاربرد و ترکیب:
- محلول آبی (Aqueous solution): محلولی است که در آن فقط آب محلل می باشد. محلول های آبی با سمبول (aq) که واژه Aqueous است نشان داده میشود. مثلا سودیم کلوراید در آب، محلول سلفوریک اسید، محلول اسیتیک اسید وغیره
- محلول بفر (Buffer Solution): محلول های آبی است که از اثر مخلوط کردن تیزاب ضعیف با قلوی مزدوج آن یا قلوی ضعیف با تیزاب مزدوج آن تشکیل میشوند. محلول های بفر در برابر تغییراتpH مقاوم اند که با تغییرات اندکی در غلظت آیون ⁺H و یا آیون هایدروکسیل ¯pH، OH محلول را نسبتا ثابت نگه میدارند، طوریکه اجزای محلول بفر با آن تعامل نموده و آیونهای اضافی را خنثی می کنند، بنابراین از تغییرات شدید در pH جلوگیری میکنند. بنا در محلول بفر تغییرات کیمیاوی نیز شامل میباشد.
در تصاویر ذیل محلول های بفری در حالات مختلف نمایش داده شده اند.
 در این تصویر، اسیتیک اسید (CH₃COOH) و آیون اسیتیت (-¯CH₃COO) در حالت تعادل قرار دارند. وقتی یک تیزاب قوی به محلول اضافه میشود، آیونهای ⁺H و با آیون اسیتیت ترکیب میشوند و اسیتیک اسید تولید میکنند، که به حفظ pH کمک میکند. برعکس، اگر یک القلی قوی اضافه شود، اسیتیک اسید آیونهای ⁺H را آزاد میکند تا pH را به حالت متعادل برگرداند.
در این تصویر، اسیتیک اسید (CH₃COOH) و آیون اسیتیت (-¯CH₃COO) در حالت تعادل قرار دارند. وقتی یک تیزاب قوی به محلول اضافه میشود، آیونهای ⁺H و با آیون اسیتیت ترکیب میشوند و اسیتیک اسید تولید میکنند، که به حفظ pH کمک میکند. برعکس، اگر یک القلی قوی اضافه شود، اسیتیک اسید آیونهای ⁺H را آزاد میکند تا pH را به حالت متعادل برگرداند.
- محلول های ایده آل (Ideal Solutions)
محلول ایده آل به مخلوطی گفته میشود که در آن 1آنتالپی تغییر نمیکند یعنی با تشکیل شدن محلول حرارت اضافی جذب و آزاد نمیشود و حجم محلول همچنان ثابت باقی میماند. در محلول ایدهآل تغییرات انتالپی مساوی با صفر است. بطور مثال: مخلوط هگزان و هپتان.
1.انتالپی نشان دهنده میزان انرژی است که به شکل حرارت در شرایط فشار ثابت از سیستم به محیط یا از محیط به سیستم منتقل میشود.
- محلول های فولک (Folch Solution): مخلوط کلوروفورم و میتانول است که در جدا سازی ترکیبات قطبی از ناقطبی کاربرد دارد. این محلول متشکل از دو مرکبی می باشند که مالیکول های آنها قطبی اند.
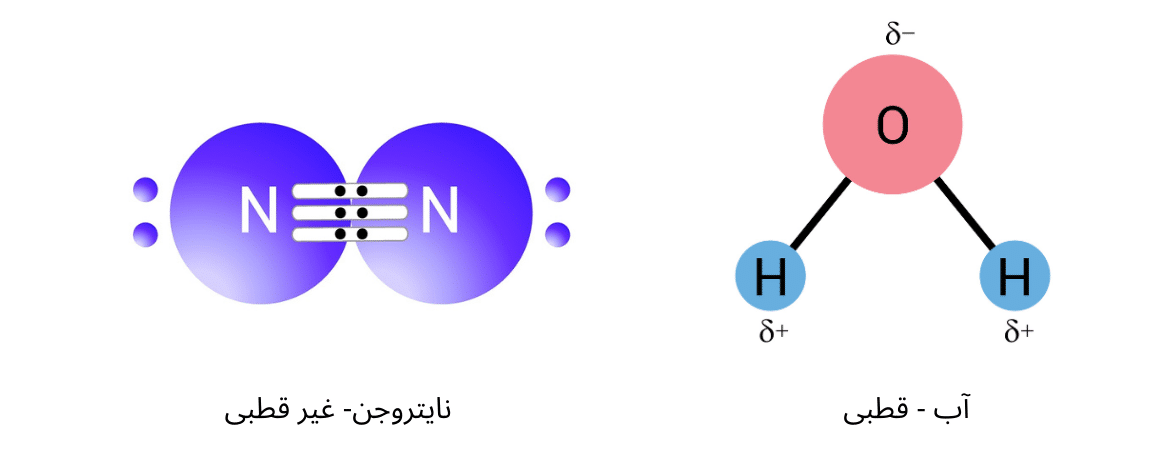
تبصره: مالیکول های قطبی به مالیکول های گفته می شوند که مالیکول در جهت اتوم الکترونیگاتیف قسما داری چارچ منفی و در جهت اتوم الکتروپاسیتیف قسما دارای چارچ مثبت باشد. به عبارت خلاصه توزیع ابر الکترونی در این نوع مالیکول ها به صورت یکسان نمی باشد. نمونه های خوبی از مالیکول های قطبی مالیکول آب و مرکب هایدروجن فلوراید می باشند. مالیکول های آب به عنوان یک مرکب قطبی قابلیت حل ساختن مالیکول های قطبی و آیونی را دارا می باشد. در مالیکول های غیر قطبی توزیع ابر الکترونی بالای اتوم های تشکیل دهنده یک مرکب یکسان می باشند. نمونه های خوبی از مالیکول های غیر قطبی مرکب میتان CH4، مالیکول های H2، O2، N2 و CO2 می باشند.
تصاویر ذیل نشان دهنده خاصیت قطبی در مالیکول آب و خاصیت غیر قطبی در مالیکول نایتروجن می باشند.
- محلول های هالتفرتر (Holtfreter’s Solution): محلول متعادل از چند نمک می باشد که برای کاهش عفونت های باکتریایی مورد استفاده قرار میگیرد. این محلول توسط زیست شناسی بنام یوهانس هولتفرتر ساخته شد. اجزای تشکیل دهنده این محلول شامل نمک های ذیل می باشد:
سودیم کلوراید NaCl
پوتاشیوم کلوراید KCl
کلسیم کلوراید CaCl2
سودیم بای کاربونیت NaHCO3
- ادبلو یا (Diesel Exhaust Fluid): محلول از 32.5 فیصد یوریا (CO(NH2)2) و 67.5 فیصد آب خالص است. که برای کاهش آلودگی هوا توسط موتورهای دیزلی مورد استفاده دارد.
محلول ها به لحاظ هدایت برقی: در این ویدیو به تشریح محلول ها به لحاظ هدایت برقی، پرداخته شده است.